Ethics and Public Policy Center. El Centro de Ética y Políticas Públicas realizó el estudio más extenso conocido sobre la píldora abortiva. Esta serie de artículos y recursos presenta los hallazgos del estudio e investiga la salud femenina y el aborto con datos reales.
- Papers
- Recursos adicionales
Los datos de seguros revelan que uno de cada diez pacientes experimenta un evento adverso grave
Resumen
- Este estudio, el más grande conocido sobre la píldora abortiva, se basa en el análisis de datos de una base de datos de reclamos de seguros de todos los pagadores que incluye 865.727 abortos prescritos con mifepristona entre 2017 y 2023.
- El 10,93 por ciento de las mujeres experimentan sepsis, infección, hemorragia u otro evento adverso grave dentro de los 45 días posteriores a un aborto con mifepristona.
- La tasa real de eventos adversos graves después de abortos con mifepristona es al menos 22 veces mayor que la cifra resumida de “menos del 0,5 por ciento” en los ensayos clínicos informada en la etiqueta del medicamento.
- La FDA debería restablecer de inmediato sus protocolos de seguridad del paciente anteriores y más estrictos para garantizar la responsabilidad de los médicos hacia las mujeres que toman mifepristona bajo su cuidado, así como exigir la notificación completa de sus efectos secundarios.
- La FDA debería investigar más a fondo el daño que causa la mifepristona a las mujeres y, basándose en criterios de seguridad objetivos, reconsiderar por completo su aprobación.
Danco Laboratories comercializa Mifeprex como «la píldora abortiva segura y eficaz», pero nuestra investigación demuestra que el aborto con mifepristona, tal como se practica actualmente en EE. UU., no es seguro ni eficaz. El fabricante y la FDA se basan en los resultados de 10 ensayos clínicos con un total de 30 966 participantes, de los cuales menos del 0,5 % experimentaron reacciones adversas graves. En cambio, analizamos datos reales de reclamaciones de seguros para 865 727 abortos con mifepristona prescritos, representativos en gran medida de las mujeres que se someten a abortos con mifepristona en EE. UU. actualmente, y encontramos una tasa de eventos adversos graves del 10,93 %, al menos 22 veces superior a la cifra resumida que figura en la etiqueta del medicamento. A la luz de esta investigación, instamos a la FDA a restablecer protocolos de seguridad para el paciente más estrictos y de forma más temprana, y a reconsiderar la aprobación de la mifepristona por completo. Las mujeres merecen algo mejor que la píldora abortiva.
Nuestros hallazgos clave
El 10,93 % de las mujeres experimentan sepsis, infección, hemorragia u otro evento adverso grave o potencialmente mortal dentro de los 45 días posteriores a un aborto con mifepristona, una cifra muy superior a la cifra general de «menos del 0,5 %» reportada en la etiqueta del medicamento en los ensayos clínicos. Figura 1 .
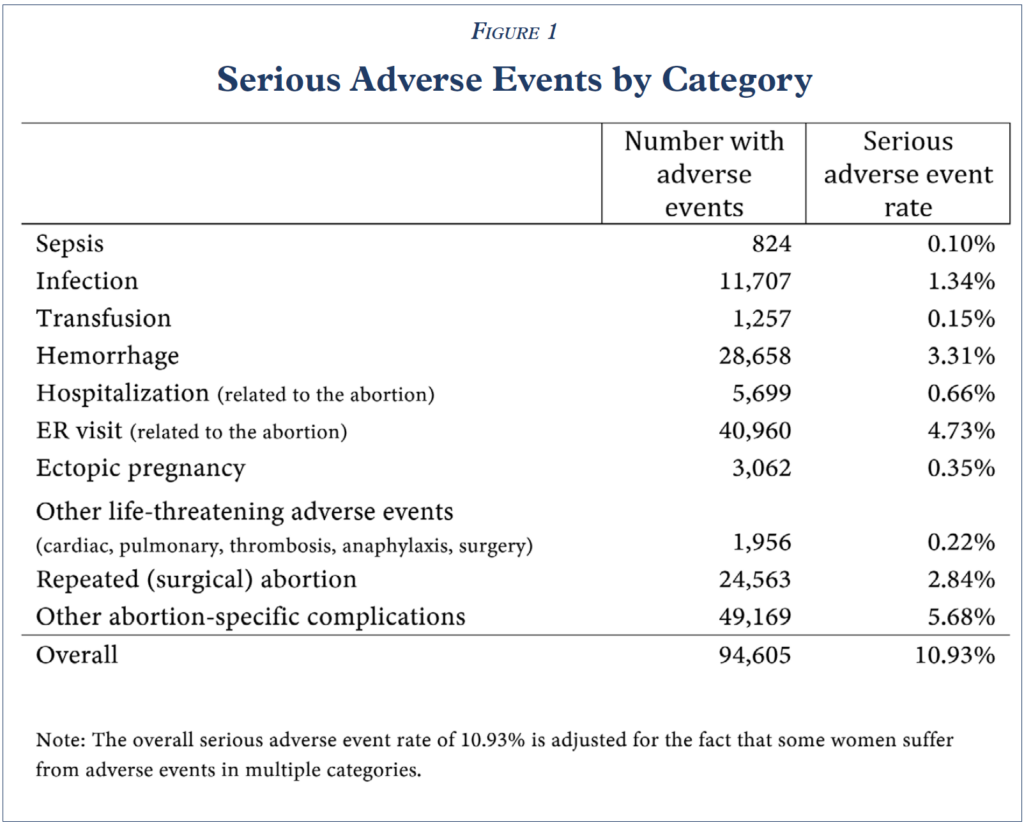
En pocas palabras, la mifepristona, tal como se usa en condiciones del mundo real, no es “segura ni eficaz”.
- Nuestro estudio observacional posterior a la comercialización en el mundo real de la mifepristona es, hasta donde sabemos, el estudio más completo sobre la seguridad del aborto químico jamás realizado en los EE. UU.:
- Identificamos e incluimos 865.727 abortos prescritos con mifepristona, 28 veces más que los incluidos en todos los ensayos clínicos citados por la FDA combinados.
- Nuestro conjunto de datos es más reciente, no anterior a 2017, mientras que la aprobación de la mifepristona por parte de la FDA se basa enteramente en datos de hace más de una década.
- Las mujeres de nuestro conjunto de datos son ampliamente representativas de las mujeres que obtienen abortos con mifepristona en los EE. UU.; no son un grupo preseleccionado de mujeres generalmente sanas reclutadas en varios ensayos clínicos realizados en diferentes momentos alrededor del mundo.
- Las mujeres de nuestro conjunto de datos reciben (o no reciben) atención médica previa y posterior al aborto de la calidad real que prevalece hoy en los EE. UU., no el régimen de atención cuidadosamente controlado que comúnmente prevalece en un ensayo clínico.
Implicaciones políticas
La FDA debería restablecer los protocolos originales de seguridad para el paciente que se exigieron cuando se aprobó la mifepristona. Esto probablemente reducirá los daños a las mujeres y permitirá un mejor seguimiento para determinar si este medicamento debe permanecer en el mercado.
- La prescripción de mifepristona y misoprostol para la interrupción del embarazo debería requerir al menos tres visitas en persona al consultorio por parte de la paciente, como lo requirió originalmente la FDA.
- La mifepristona debe ser recetada únicamente por médicos (como lo exigió originalmente la FDA) que hayan leído y comprendido la información de prescripción.
- La mifepristona debe administrarse únicamente en una clínica, consultorio médico u hospital, por o bajo la supervisión de un médico, capaz de evaluar la edad gestacional de un embrión y diagnosticar embarazos ectópicos, todo lo cual fue originalmente requerido por la FDA.
- Los médicos deben poder proporcionar intervención quirúrgica en casos de aborto incompleto o sangrado severo, o haber hecho planes para brindar dicha atención a través de otros, y poder asegurar el acceso de los pacientes a instalaciones médicas equipadas para proporcionar transfusiones de sangre y reanimación, si es necesario.
- Se debería exigir nuevamente a los proveedores de atención médica que informen a la FDA (y a los fabricantes de mifepristona) todos los eventos adversos graves resultantes del uso de mifepristona.
- La mifepristona sólo debe recetarse a una mujer que, según lo confirmado por un médico, se encuentra en las primeras siete semanas de embarazo, como lo exigió originalmente la FDA.
Antecedentes sobre la aprobación y regulación de la mifepristona por parte de la FDA
La mifepristona fue desarrollada por la farmacéutica francesa Roussel Uclaf SA e introducida en Estados Unidos a instancias del presidente Clinton y tras la presión del Congreso. La FDA la aprobó mediante un proceso de aprobación poco utilizado para «ciertos medicamentos nuevos que han sido estudiados por su seguridad y eficacia en el tratamiento de enfermedades graves o potencialmente mortales y que proporcionan un beneficio terapéutico significativo a los pacientes en comparación con los tratamientos existentes». Por lo tanto, para otorgar esta aprobación, la FDA tuvo que considerar un embarazo no deseado como una «enfermedad grave o potencialmente mortal» y determinar que la mifepristona era más eficaz que el aborto quirúrgico en su tratamiento. La decisión de la FDA cita datos mínimos: ensayos clínicos con solo 859 participantes en EE. UU. y 1800 en Francia.
La etiqueta original del medicamento Mifeprex (nombre comercial de la mifepristona), aprobada por la FDA en septiembre de 2000, indicaba su uso para la interrupción médica del embarazo intrauterino hasta los 49 días de gestación. Exigía varias medidas de protección para la salud de la mujer:
El tratamiento con Mifeprex y misoprostol para la interrupción del embarazo requiere tres visitas al consultorio de la paciente. Mifeprex debe ser recetado únicamente por médicos que hayan leído y comprendido la información de prescripción. Mifeprex solo puede administrarse en una clínica, consultorio u hospital, por o bajo la supervisión de un médico capaz de evaluar la edad gestacional del embrión y diagnosticar embarazos ectópicos. Los médicos también deben ser capaces de realizar intervenciones quirúrgicas en casos de aborto incompleto o sangrado grave, o haber planificado brindar dicha atención a través de otros, y poder garantizar el acceso de la paciente a instalaciones médicas equipadas para realizar transfusiones de sangre y reanimación, de ser necesario.
Durante las administraciones de Obama y Biden, la FDA desmanteló estas salvaguardas iniciales, poniendo en riesgo la salud de las mujeres para ampliar el acceso al aborto. Según la Estrategia de Evaluación y Mitigación de Riesgos (REMS), vigente desde 2023:
- Un aborto con mifepristona ahora requiere tan solo una visita de telesalud con cualquier proveedor de atención médica aprobado (no necesariamente un médico),
- Una mujer puede autoadministrarse medicamentos obtenidos en una farmacia por correo, y
- El médico prescriptor no está obligado a notificar ningún evento adverso a menos que sepa que un paciente ha fallecido. Figura 2.
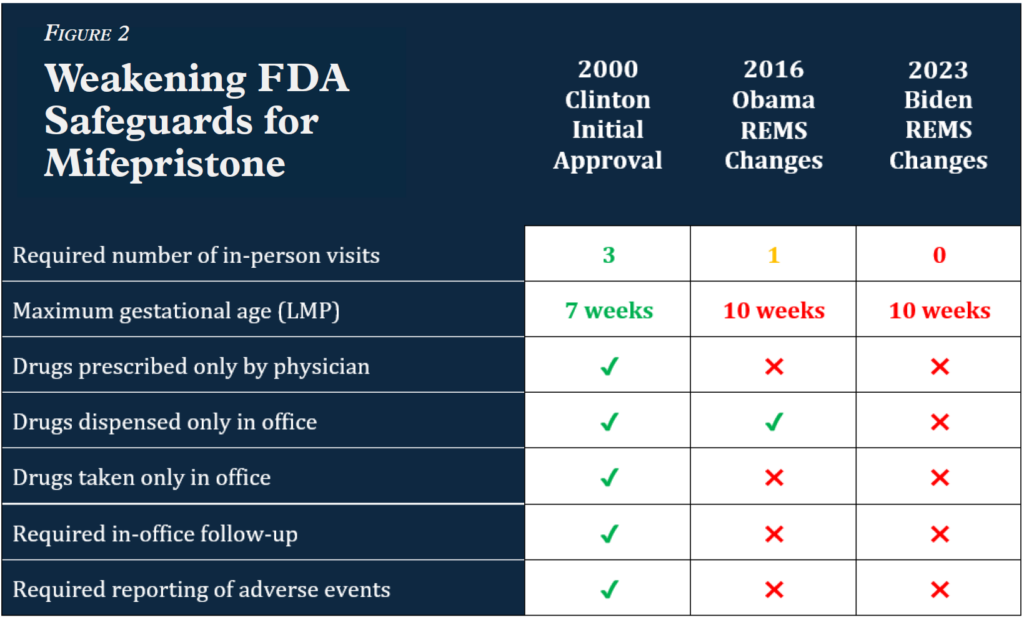
La ficha técnica actual del medicamento aprobada por la FDA se refiere a los resultados de 10 ensayos clínicos con un total de 30 966 participantes, de los cuales menos del 0,5 % experimentaron reacciones adversas graves. Sin embargo, estas cifras se basan exclusivamente en datos de ensayos realizados hace más de una década.
La creciente cuota de mercado del aborto químico
El mayor acceso al aborto químico ha coincidido con un rápido aumento de su prevalencia. Los abortos químicos —la gran mayoría de los cuales se realizan con una combinación de mifepristona y misoprostol— representan actualmente aproximadamente dos tercios de todos los abortos en Estados Unidos. Figura 3.
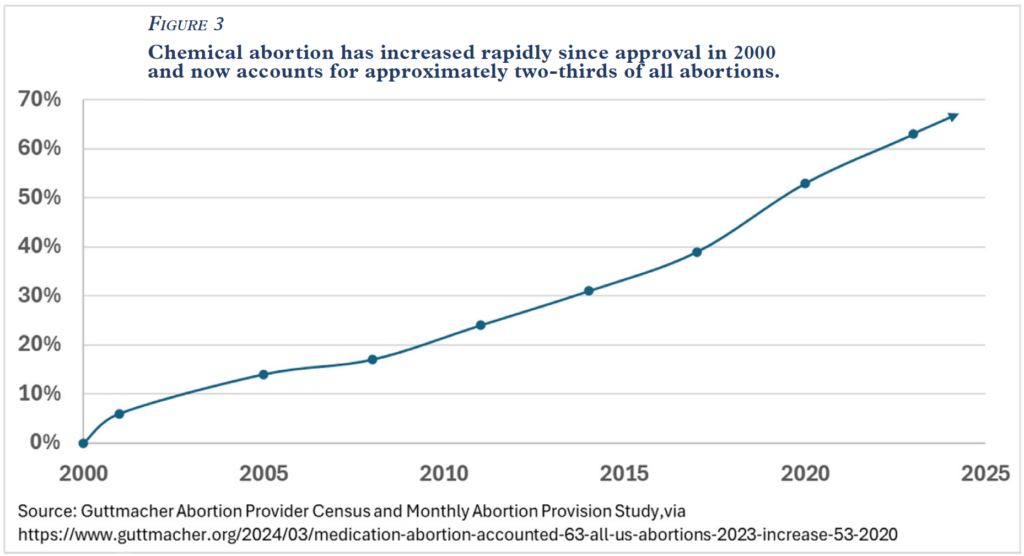
De hecho, Danco Laboratories se jacta de que más de 5 millones de mujeres estadounidenses han usado su píldora abortiva desde que fue aprobada en 2000. Por lo tanto, se ha vuelto cada vez más importante comprender los riesgos y los daños que el aborto químico en general y la mifepristona en particular suponen para las mujeres.
Cómo identificamos los abortos con mifepristona
En nuestros datos, un aborto con mifepristona se identificó de una de tres maneras:
- Código de procedimiento S0199: aborto inducido médicamente mediante la ingestión oral de medicamentos, incluidos todos los servicios y suministros asociados.
- una receta para mifepristona (con o sin misoprostol dentro de los próximos 3 días), o
- un código de diagnóstico para interrupción electiva o embarazo no deseado, junto con otros códigos de facturación consistentes con las instrucciones del fabricante para el reembolso de un aborto con mifepristona para una combinación determinada de estado y aseguradora.
Siguiendo este método, identificamos un total de 865.727 abortos con mifepristona prescritos para un total de 692.873 mujeres entre 2017 y 2023. Esto incluye 566.446 mujeres, cada una de las cuales tuvo un aborto de este tipo, y 126.427 mujeres con múltiples abortos de este tipo.
Cómo identificamos eventos adversos graves
Seguimos la definición oficial de la FDA de «evento adverso grave». Para ello, identificamos los códigos de diagnóstico CIE-10 y los códigos de procedimiento CPT/HCPCS relevantes para eventos adversos de diversas fuentes:
- Indicadores de morbilidad materna grave (SMM) de los CDC,
- Códigos 770 y 769 del Grupo Relacionado con el Diagnóstico (DRG) de CMS,
- Informes del Sistema de notificación de eventos adversos de la FDA (FAERS) (interpretados y traducidos a códigos de diagnóstico y procedimiento por los médicos de nuestro equipo), y
- un pequeño número de códigos (en su mayoría ginecológicos) sugeridos por nuestros médicos.
Estos códigos fueron calificados por un equipo de médicos utilizando los Criterios Terminológicos Comunes para Eventos Adversos de los NIH (CTCAE versión 5), que categorizan los eventos adversos según su gravedad en una escala de 5 puntos. Incluimos los grados 3 (graves) y 4 (potencialmente mortales) de los CTCAE. No incluimos los grados 1 (leves) ni 2 (moderados). (El grado 5 corresponde a la muerte, que se consideraría un evento adverso grave según la definición de la FDA, pero no necesariamente se observó en los datos de reclamaciones de seguros. Esperamos mostrar la tasa de mortalidad en un informe posterior).
Para los informes, hemos agrupado los códigos de diagnóstico y procedimiento relevantes de la siguiente manera:
- La ficha técnica de mifepristona divide los eventos adversos graves en seis categorías identificadas en los ensayos clínicos: sepsis, infección, transfusión, hemorragia, hospitalización y visita a urgencias. Nuestro análisis solo incluye las hospitalizaciones y visitas a urgencias con códigos de diagnóstico y procedimiento relacionados con el aborto.
- FAERS recibió informes de varios eventos que nuestros médicos consideran potencialmente mortales y los han agrupado en categorías amplias: embarazo ectópico, cirugía, cardíacos, pulmonares, trombosis y anafilaxia.
- Los procedimientos de aborto (quirúrgicos) repetidos se consideran eventos adversos graves.
- Otras complicaciones del aborto incluyen códigos específicamente relacionados con un aborto o aborto espontáneo, así como diagnósticos de salud mental potencialmente mortales, etc.
Solo consideramos los eventos adversos graves ocurridos dentro de los 45 días posteriores al aborto. Esto es conservador, ya que algunos eventos adversos pueden presentarse más tarde (y los estudios en los que se basa la FDA utilizaron un período de hasta 72 días). Además, la probabilidad de un embarazo posterior dentro de este período es insignificante, lo que garantiza que los eventos adversos estén relacionados con el aborto y no con un embarazo posterior.
Nuestros datos
Nuestro equipo ha adquirido acceso a una base de datos de reclamaciones de seguros médicos de todo pagador, disponible comercialmente, que incluye datos anónimos de todos los pacientes estadounidenses entre 2017 y 2023. Esta base de datos incluye información sobre visitas a hospitales y consultorios, diagnósticos, procedimientos y recetas procesadas a través de seguros médicos privados, Medicaid, Medicare, TRICARE y el Departamento de Asuntos de Veteranos (VA). Los datos excluyen las transacciones en las que la aseguradora también es proveedora (como ocurre con algunas HMO y gran parte de la atención del VA), así como las transacciones de pago en efectivo (que son desproporcionadamente comunes en el caso de abortos). Este conjunto de datos proporciona un seguimiento longitudinal de los diagnósticos, procedimientos y recetas médicas de cada paciente y se utiliza ampliamente en la investigación académica y regulatoria.
Nuestro equipo de proyectos de investigación
Nuestro proyecto de investigación fue realizado y validado por un equipo de científicos de datos, analistas e ingenieros, con la asistencia de nuestro equipo clínico de obstetras y ginecólogos certificados. Nuestros miembros cuentan con una amplia trayectoria en investigación académica y publicaciones revisadas por pares.
Conclusión
Nuestra investigación demuestra inequívocamente que el aborto con mifepristona, tal como se practica actualmente en EE. UU., es considerablemente más peligroso para las mujeres de lo que indica la etiqueta del medicamento aprobado por la FDA. La FDA debería restablecer de inmediato sus protocolos de seguridad para el paciente, que eran anteriores y más estrictos, para garantizar la responsabilidad médica de las mujeres que toman mifepristona bajo su cuidado, así como exigir la notificación completa de sus efectos secundarios. La FDA debería investigar más a fondo los daños que este medicamento causa a las mujeres y, basándose en criterios objetivos de seguridad, reconsiderar su aprobación por completo. Las mujeres merecen algo mejor que la píldora abortiva.
Datos de seguros revelan repetidos intentos de aborto debido a alta tasa de fracaso
Resumen
- La tasa de fracaso en el mundo real del aborto con mifepristona (al menos 5,26 por ciento, o aproximadamente uno de cada 19 casos) es el doble de la tasa de fracaso de los ensayos clínicos estadounidenses y aproximadamente dos tercios más alta que la tasa de fracaso combinada de todos los ensayos clínicos informados en la etiqueta del medicamento aprobado por la FDA.
- Combinado con nuestro hallazgo anterior de que el 10,93 por ciento de las mujeres experimentan un evento adverso grave y ajustando para evitar el doble conteo, encontramos que el 13,51 por ciento de las mujeres (aproximadamente una de cada siete) experimentan al menos un evento adverso grave o un intento repetido de aborto dentro de los 45 días posteriores al primer intento de aborto con mifepristona.
- Este estudio, el más grande conocido sobre la píldora abortiva, se basa en el análisis de datos de una base de datos de reclamos de seguros de todos los pagadores que incluye 865.727 abortos prescritos con mifepristona entre 2017 y 2023.
- La FDA debería restablecer de inmediato sus protocolos de seguridad del paciente anteriores y más estrictos para garantizar la responsabilidad de los médicos hacia las mujeres que toman mifepristona bajo su cuidado, así como exigir la notificación completa de sus efectos secundarios.
- La FDA debería investigar más a fondo el daño que este medicamento causa a las mujeres y, basándose en criterios objetivos de seguridad y eficacia, reconsiderar por completo su aprobación.
Danco Laboratories comercializa Mifeprex como «la píldora abortiva segura y efectiva», pero nuestra investigación muestra que el aborto con mifepristona, como se practica actualmente en los EE. UU., no es seguro ni efectivo . El fabricante y la FDA se basan en los resultados de ensayos clínicos en los que menos del 0.5 por ciento de los participantes experimentaron reacciones adversas graves y todos, excepto el 2.6-3.8 por ciento, obtuvieron un aborto completo al tomar mifepristona más misoprostol . Por el contrario, analizamos datos de reclamos de seguros del mundo real para 865,727 abortos con mifepristona prescritos, ampliamente representativos de las mujeres que obtienen abortos con mifepristona en los EE. UU. hoy, y encontramos una tasa de eventos adversos graves del 10.93 por ciento y una tasa de fracaso de al menos el 5.26 por ciento. A la luz de esta investigación, instamos a la FDA a restablecer protocolos de seguridad para el paciente más tempranos y más fuertes y reconsiderar su aprobación de la mifepristona en general. Las mujeres merecen algo mejor que la píldora abortiva.
Intentos repetidos de aborto tras el fracaso del régimen abortivo con mifepristona
Según los datos del seguro, el 5,26 por ciento de las mujeres se someten a un segundo intento de aborto dentro de los 45 días del primero, lo que indica que el primer intento de aborto con mifepristona fracasó. ( También observamos que al 1,58 por ciento de las mujeres se les prescribe una segunda dosis de misoprostol, pero no una segunda dosis de mifepristona, una posibilidad sugerida en la etiqueta del medicamento para los casos en que la mujer ya no está embarazada, pero los restos fetales no han sido expulsados completamente de su cuerpo. Estos no se cuentan como intentos de aborto repetidos, pero el uso repetido de misoprostol tiene efectos secundarios que suponen un mayor daño para las mujeres ). Curiosamente, aunque la etiqueta del medicamento no parece contemplar la posibilidad de un segundo intento de aborto utilizando mifepristona para el mismo embarazo, observamos esto regularmente en la base de datos de reclamaciones de seguros. Consulte la Tabla 1.

La tasa de fracaso real del aborto con mifepristona (al menos el 5,26 %, o aproximadamente uno de cada 19 casos) duplica la tasa de fracaso del 2,6 % de los ensayos clínicos estadounidenses y es aproximadamente dos tercios mayor que la tasa de fracaso combinada del 3,2 % de todos los ensayos clínicos, según lo informado en la ficha técnica del medicamento aprobado por la FDA. ( No consideramos aquí los casos en los que una mujer dio a luz tras un intento de aborto con mifepristona, lo que, técnicamente, también indica que el régimen no funcionó según lo previsto. Si también se incluyeran estos casos, la tasa de fracaso sería ligeramente mayor ) .
(La Tabla 3 en la página 13 de la etiqueta del medicamento informa la intervención quirúrgica en el 2,6 por ciento de 16.794 casos en ensayos en EE. UU. y en el 3,8 por ciento de 18.425 casos en ensayos fuera de EE. UU. Esto equivale en promedio al 3,2 por ciento de 35.219 casos en general. Consulte la etiqueta del medicamento Mifeprex (mifepristona) )
Seguridad y eficacia
Como informamos previamente , el 10,93 % de las mujeres (aproximadamente una de cada diez) experimenta sepsis, infección, hemorragia u otro evento adverso grave dentro de los 45 días posteriores a un aborto con mifepristona. Si sumamos el 5,26 % de mujeres que se someten a un segundo intento de aborto tras el fracaso del régimen de aborto con mifepristona, y ajustando para evitar la doble contabilización, observamos que el 13,51 % de las mujeres (aproximadamente una de cada siete) experimenta al menos un evento adverso grave o un segundo intento de aborto dentro de los 45 días posteriores al primer intento de aborto con mifepristona. Véase la Tabla 2.

Conclusión
El aborto con mifepristona, tal como se practica actualmente en EE. UU., no es seguro ni eficaz. Como demostró nuestro artículo anterior, la tasa real de eventos adversos graves tras un aborto con mifepristona es al menos 22 veces superior a la indicada en la etiqueta del medicamento. Ahora, también descubrimos que su tasa de fracaso es significativamente mayor. En total, aproximadamente una de cada siete mujeres a las que se les prescribe un aborto con mifepristona experimenta un evento adverso grave o se somete a un nuevo intento de aborto poco después debido al fracaso del régimen de aborto con mifepristona.
A la luz de estos hallazgos, la FDA debería restablecer de inmediato sus protocolos de seguridad para el paciente, que eran anteriores y más estrictos, para garantizar la responsabilidad médica de las mujeres que toman mifepristona bajo su cuidado, así como exigir la notificación completa de sus efectos secundarios. La FDA debería investigar más a fondo los daños que este medicamento causa a las mujeres y, basándose en criterios objetivos de seguridad y eficacia, reconsiderar su aprobación por completo. Las mujeres merecen saber la verdad. Las mujeres merecen algo mejor que la píldora abortiva.
